AJUSTE DE REACCIONES QUÍMICAS
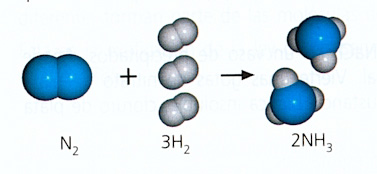
Tipos de reacciones químicas
Las reacciones químicas son las transformaciones de la materia que producen cambios en unas sustancias para obtener otras diferentes.
En estas transformaciones, se parte de unas sustancias en el estado inicial, llamadas reactivos, y se obtienen otras diferentes en el estado final, llamadas productos.
Aunque existen muchas y muy variadas formas de clasificar las reacciones en fase acuosa, hay tres tipos de reacciones que pueden catalogarse como las más importantes desde el punto de vista ambiental.
Estas son las Reacciones de Precipitación, las Reacciones Ácido-Base y las Reacciones Redox.
Reacciones de precipitación
Son reacciones que se caracterizan por la formación de un producto insoluble o precipitado siendo éste el producto de la reacción. Un ejemplo es cuando se mezclan soluciones de NaCl y AgNO3, se forma el cloruro de plata, AgCl, producto insoluble y NaNO3:
NaCl + AgNO3 = AgCl + NaNO3
Reacciones ácido-base
Son reacciones en las que se combina un ácido con una base para dar una sal y agua. Un ejemplo de estas es la unión de HCl con NaOH, formándose NaCl y agua:
HCl + NaOH = NaCl + H2P
Reacciones Redox
También llamadas de óxido-reducción, son reacciones de intercambio de electrones y en ellas ocurre una variación del número de oxidación de los productos respecto a los reactivos. Así, por ejemplo, el proceso siderúrgico de producción de hierro puede representarse mediante las siguientes dos "Semi-Reacciones":
| Semi-reacción de Reducción | 2Fe2O3 = 4Fe + 3O2 |
| Semi-reacción de Oxidación | 2CO + O2 = 2CO2 |
| Reacción General | 2Fe2 + 2CO = Fe + CO2 |